3. Das AMNOG-Verfahren: mehr als nur Kostenkontrolle
In Deutschland gibt es keine vierte Hürde für neue Arzneimittel. Eine Kosten-Nutzen-Analyse spielt in der frühen Nutzenbewertung nach dem Arzneimittelmarktneuordnungsgesetz (AMNOG) keine zentrale Rolle und ist regulativ auch nicht als Schwelle für den Marktzugang vorgesehen. Daher wird derzeit auch keinem Mittel wegen eines schlechten Kosten-Nutzen-Verhältnisses der Zugang zum Markt in Deutschland verwehrt.
Das primäre Ziel der frühen Nutzenbewertung ist also nicht die Begrenzung des Marktzugangs, sondern die Kostenkontrolle. Bis zum Inkrafttreten des AMNOG im Jahr 2011 konnten die Hersteller die Preise für neue Arzneimittel relativ frei festlegen – ohne Nutzennachweis. Die frühe Nutzenbewertung nach dem AMNOG macht den Erstattungspreis eines neuen Wirkstoffs nach Ablauf der ersten 6 Monate abhängig vom nachgewiesenen Zusatznutzen im Vergleich zur sogenannten zweckmäßigen Vergleichstherapie, also der Standardtherapie. Ist dieser nicht nachweisbar, kann nur der Preis erstattet werden, den die gesetzlichen Krankenkassen auch für das Standardpräparat bezahlen. Die so erzielten jährlichen Einsparungen für die gesetzliche Krankenversicherung beziffert die DAK in ihrem AMNOG-Report für das Jahr 2019 auf mehr als drei Milliarden Euro.
Über die nutzenbasierte Preisfindung patentgeschützter Arzneimittel hinaus ergeben sich aus dem AMNOG weitere positive Effekte im Vergleich zu den Verhältnissen in anderen Ländern:
Da jeder neue Wirkstoff in Deutschland das AMNOG-Verfahren verpflichtend durchlaufen muss, bewertet für jedes Mittel mit Ausnahme der sogenannten Orphan Drugs eine unabhängige Stelle, das IQWiG, den patientenrelevanten Nutzen. (Bei Orphan Drugs, also Wirkstoffen zur Behandlung seltener Erkrankungen, gilt ein Zusatznutzen rechtlich als gegeben, und der Gemeinsame Bundesausschuss, kurz G-BA, befindet über dessen Ausmaß.) Das ermöglicht es der Ärztin oder dem Arzt, sich ausführlich über Nutzen und Risiken des neuen Wirkstoffs zu informieren, bevor sie bzw. er es seinen Patienten verordnet.
Zugleich schafft das AMNOG-Verfahren einen Grad an Transparenz, den es so kaum in anderen Ländern gibt. So sind die Hersteller dazu verpflichtet, im Dossier für den neuen Wirkstoff ihre Studienergebnisse offenzulegen. Das Transparenzprinzip gilt auch für den G-BA und das IQWiG. Die Dossierbewertungen des IQWiG und die Beschlüsse des G-BA sind öffentlich, wie auch der Meinungsbildungsprozess im Plenum auf dem Weg zu einer Entscheidung im G-BA.
Auch wenn die Kostenkontrolle im Fokus des AMNOG steht, hat das Verfahren durchaus Einfluss darauf, wie weit sich ein Wirkstoff auf dem Markt etabliert. Denn Ärztinnen und Ärzte können auf Basis der frei verfügbaren und unabhängigen Informationen über die Wirkungsweise, den Zusatznutzen und die Risiken eines Wirkstoffs entscheiden, welches Mittel sie ihren Patientinnen und Patienten verordnen.
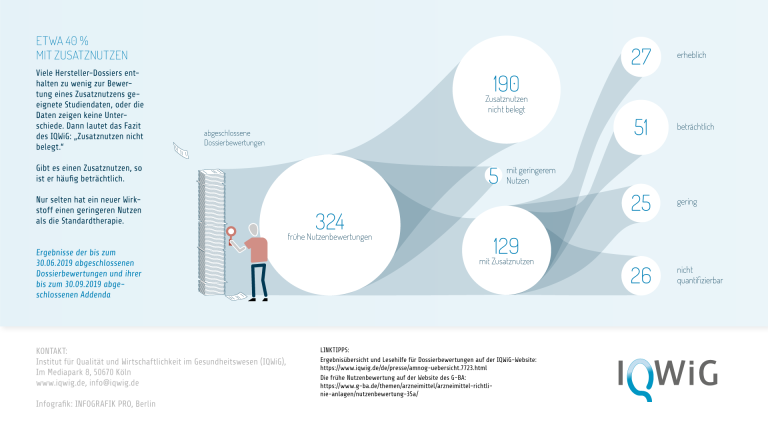
Schließlich liefert die ausführliche Analyse der frühen Nutzenbewertung Ansatzpunkte, mit denen auch der Zulassungsprozess durch die EMA verbessert werden kann. So zeigt etwa eine Auswertung von 216 IQWiG-Nutzenbewertungen neuer Arzneimittel aus den Jahren 2011 bis 2017 (Wieseler et al. 2019), von denen fast alle durch die EMA für den europäischen Markt zugelassen worden waren, dass bei mehr als der Hälfte kein Zusatznutzen ermittelt werden konnte . Lediglich in 54 (25 %) der Bewertungen ergab sich ein erheblicher oder beträchtlicher Zusatznutzen. Solche Analysen können eine Diskussion darüber anstoßen, wie sich die Zahl echter Innovationen im Arzneimittelbereich nicht nur in Deutschland, sondern in der gesamten EU spürbar steigern ließe.
Neue Arzneimittel: Zulassung, Nutzenbewertung, Erstattung
1. Arzneimittel-Zulassung und frühe Nutzenbewertung in Deutschland
2. Arzneimittel-Zulassung und -Nutzenbewertung in anderen Ländern
3. Das AMNOG-Verfahren: mehr als nur Kostenkontrolle
4. Besondere Therapierichtungen und traditionelle Arzneimittel